Химия. 11 класс
Химические свойства металлов: взаимодействие с кислородом, галогенами, серой и отношение к воде, кислот, солей. Химические свойства металлов обусловлены способностью их атомов легко отдавать электроны с внешнего энергетического уровня , превращаясь в положительно заряженные ионы. Таким образом в химических реакциях металлы проявляют себя энергичными восстановителями. Это является их главной общей химической свойством.
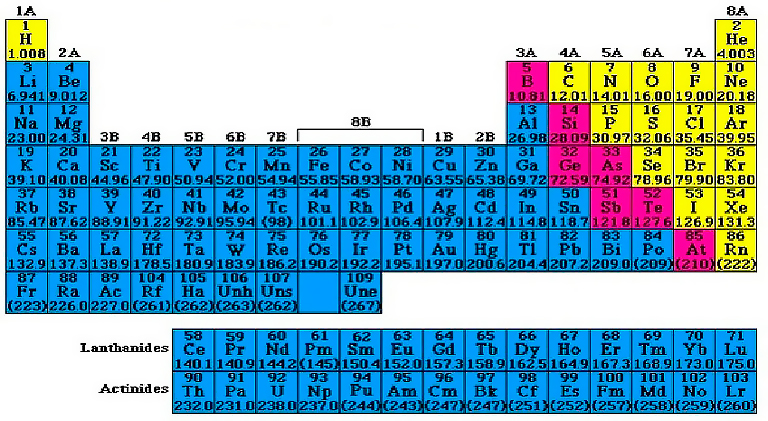







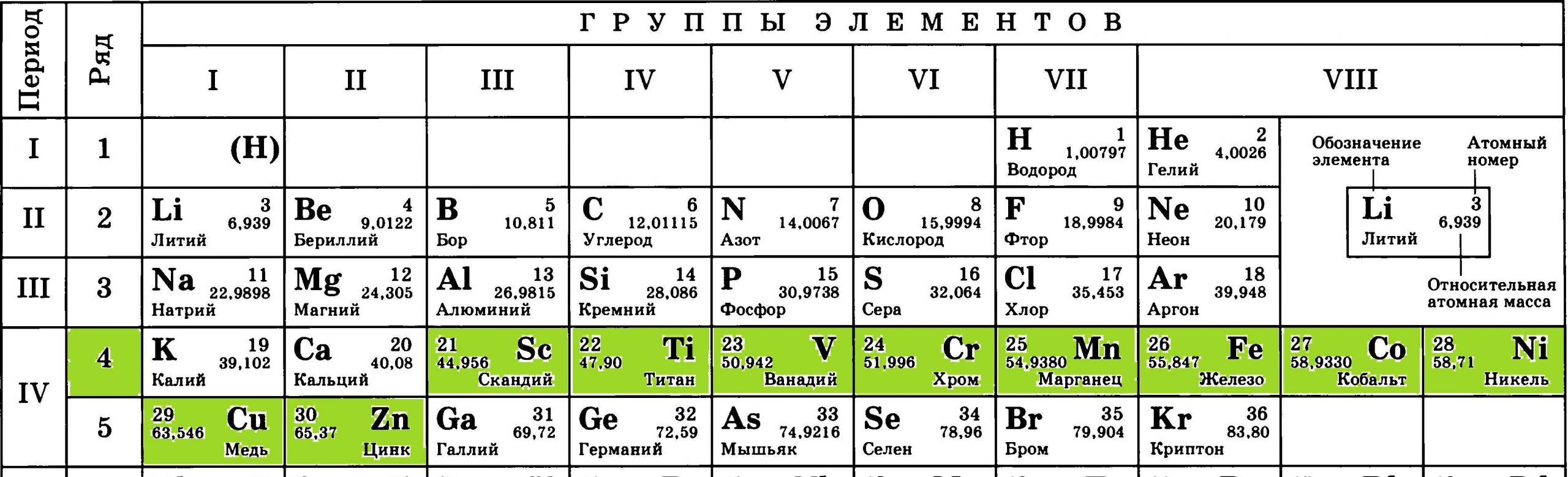
Здравствуй, читатель! В этой же статье мы поговорим о химических свойствах металлов. Если в периодической таблице элементов Д. Менделеева провести диагональ от бериллия к астату , то под диагональю будут находиться металлы к ним же относятся элементы побочных подгрупп, выделены синим цветом , а над ней — неметаллы выделены красным цветом.







По химическим свойствам металлы являются восстановителями, так как легко отдают свои электроны атомам неметаллов, превращаясь в положительно заряженные ионы — катионы. Способность атомов металлов отдавать, а их катионов — присоединять электроны может служить мерой их химической активности. Так, алюминий на воздухе очень быстро покрывается оксидной плёнкой, а с золотом заметных изменений не происходит. Цинк активно взаимодействует с соляной кислотой, а серебро — нет. Поэтому алюминий и цинк можно отнести к активным металлам, а золото и серебро — к неактивным. Химическую активность разных металлов легко сопоставить, анализируя их поведение в водных растворах солей и кислот.








