Sorry, your request has been denied.
Процессы переноса в газах могут быть описаны с использованием молекулярно-кинетической теории. Такое описание дает правильные выражения для уравнений переноса и приближенные с точность до постоянного множителя порядка единицы формулы для расчета коэффициентов переноса. Полученные значения для коэффициентов переноса оказываются несколько заниженными по сравнению с их выражениями, получаемыми при точных расчетах, которые обычно проводятся с использованием методов статистической физики. Будем считать, что молекулы газа совершают хаотическое тепловое движение.


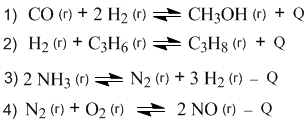




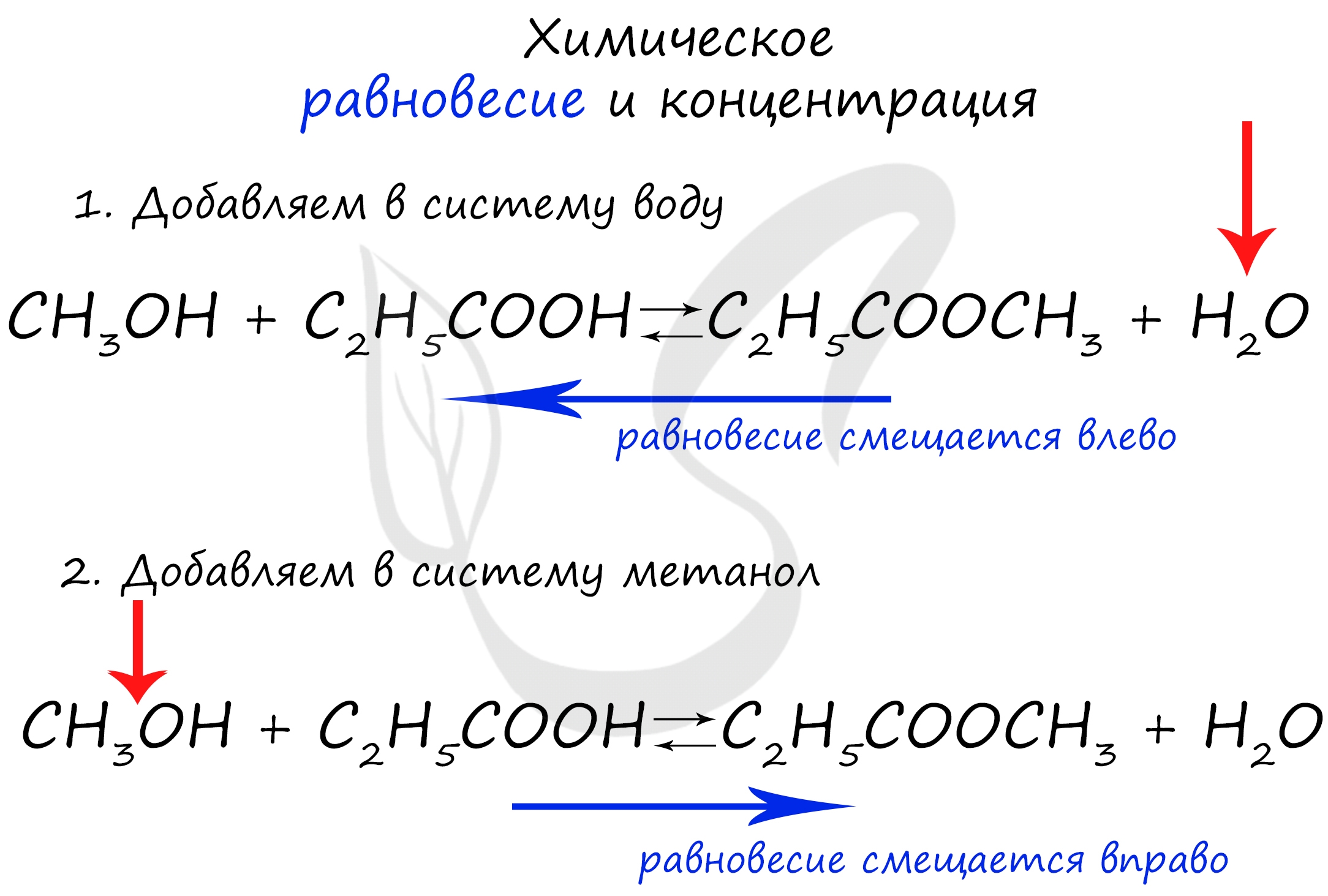
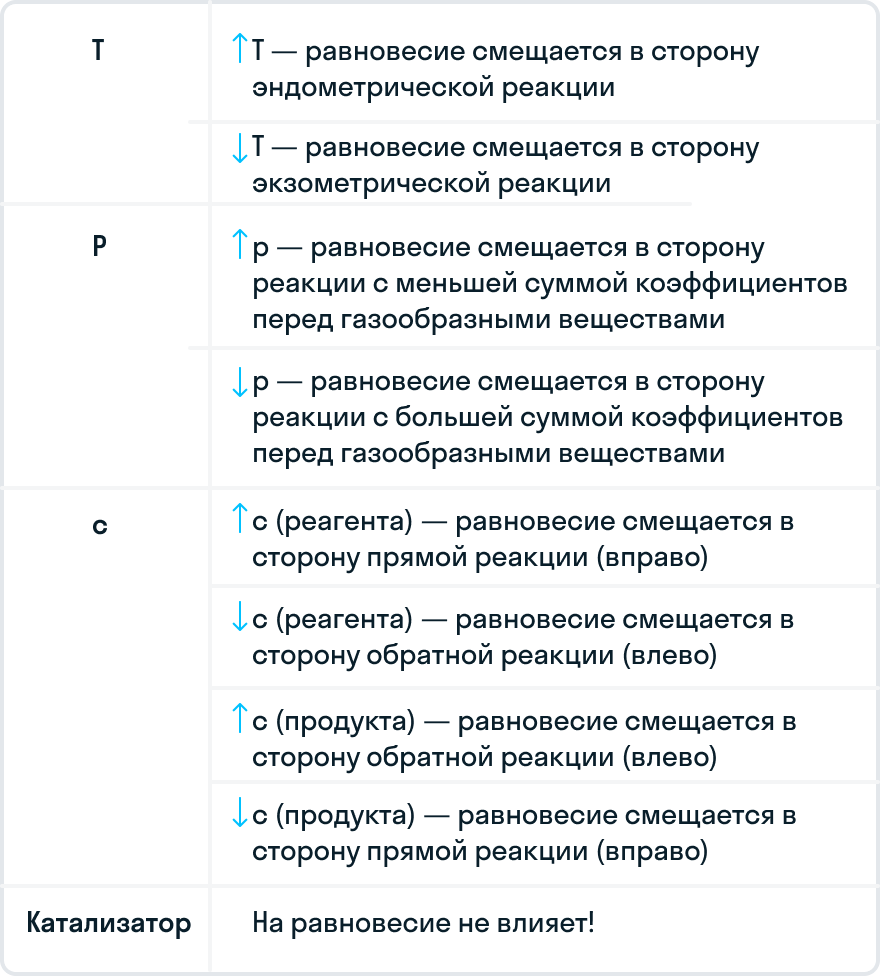
Химическое равновесие — состояние химического обратимого процесса, при котором скорость прямой реакции равна скорости обратной реакции. Для системы, находящейся в химическом равновесии, концентрации реагентов , температура и другие параметры системы не изменяются со временем [1]. Положение химического равновесия зависит от следующих параметров реакции: температуры , давления и концентрации. Влияние, которое оказывают эти факторы на химическую реакцию, подчиняется закономерности, которая была высказана в общем виде в году французским учёным Ле Шателье.
- Будущий технарь. Подготовка к ЕГЭ по физике.
- Вход Регистрация.
- Анри Ле Шателье Франция сформулировал этот термодинамический принцип подвижного равновесия, позже обобщённый Карлом Брауном [1]. Принцип применим к равновесию любой природы: механическому, тепловому, химическому, электрическому эффект Ленца , явление Пельтье [2].
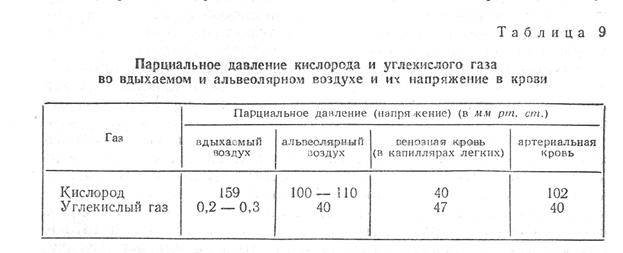
- Явление самопроизвольного изменения концентрации какого-либо вещества у поверхности раздела двух фаз называется сорбцией. Повышение концентрации газообразного или растворенного вещества на поверхности раздела фаз, например, на поверхности раздела твердое тело — газ, твердое тело — раствор, жидкость — газ воздух называется адсорбцией.
- Вход Регистрация. Учебные заведения.
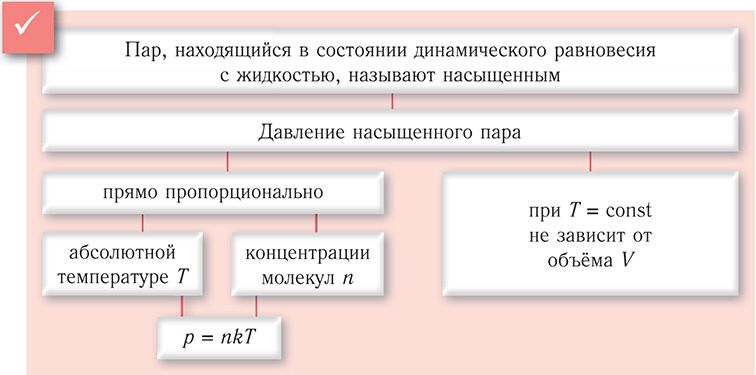
- При изучении физики мы нередко сталкиваемся с понятием давления газа.
- Как изменилась концентрация молекул газа?
- Основы МКТ.
- Изменение давления газа путем изменения его объема является одним из важнейших принципов физики.




![Описание явлений переноса в газах [ М Г Т У ]](https://otvetto.ru/wp-content/uploads/kasm4-1.png)
/Mansurov.files/image001.png)
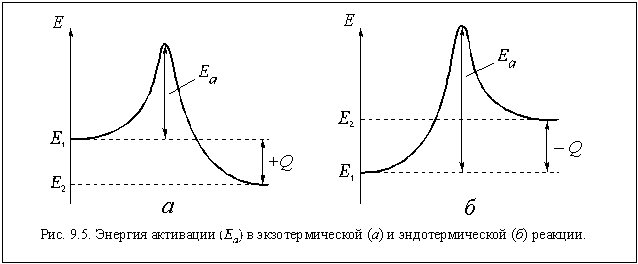

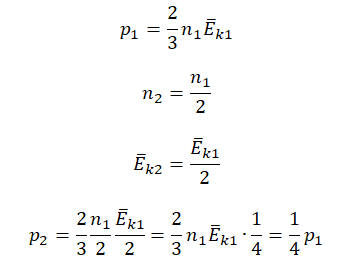
Уравнение Клапейрона-Менделеева достаточно хорошо описывает газ при высоких температурах и низких давлениях, когда он находится в условиях достаточно далёких от условий конденсации. Однако для реального газа это не всегда выполняется и тогда приходится учитывать потенциальную энергию взаимодействия молекул газа между собой. Простейшим уравнением состояния, описывающим неидеальный газ, является уравнение, предложенное в г. Иоханнесом Дедериком Ван-дер-Ваальсом - :. Для различных газов они различны, и их можно определить экспериментально. Значение константы такое же, как и для идеального газа.